МАСТОПАТИЯ В ПРАКТИКЕ АКУШЕРА-ГИНЕКОЛОГА
В.Н. Прилепская, д.м.н., проф., засл. деятель пауки РФ,
Т. Т. Тагиева, д.м.н. ФГУ Научный центр акушерства, гинекологии и перинатологии Росмедтехнологий, Москва
В статье рассматриваются вопросы клиники и лечения фиброзно-кистозной болезни (ФКБ, кистозной мастопатии) молочных желез (МЖ) в практике акушера-гинеколога. Даются современные представления об этиопатогенезе ФКБ и связи доброкачественной патологии МЖ с раком МЖ. Представлены результаты клинического изучения негормонального лекарственного препарата «Мамоклам» у 31 больной ФКБ. Выявлен значительный лечебный эффект мамоклама у пациенток с диффузными формами ФКБ.
Мастопатия или фиброзно-кистозная болезнь (ФКБ) молочных желез (МЖ) как заболевание впервые была описана в начале прошлого века. В настоящее время наблюдается стойкая тенденция к росту доброкачественных заболеваний МЖ, и данная патология часто встречается в практике акушера-гинеколога. Изучение демографических аспектов эпидемиологии заболеваний МЖ показывает, что репродуктивное поведение, характеризующееся снижением числа родов, поздним деторождением, большим количеством абортов, укорочением периода грудною вскармливания во многом определяет рост заболеваемости ФКБ [14,22, 23, 28].
По определению ВОЗ (1984), мастопатия — это фиброзно-кистозная болезнь, характеризующаяся нарушением соотношений эпителиального и соединительнотканного компонентов, широким спектром пролиферативных и регрессивных изменений тканей МЖ. Существует большое число классификаций мастопатии. В клинической практике наиболее часто используют клинико-рентгенологический вариант классификации, предложенный Н.И. Рожковой в 1983 году.
Диффузная форма фиброзно-кистозной мастопатии:
• диффузная мастопатия с преобладанием кистозного компонента;
• диффузная мастопатия с преобладанием фиброзного компонента;
• диффузная мастопатия с преобладанием железистого компонента;
• смешанная форма диффузной мастопатии;
• склерозирующий аденоз.
Узловая форма фиброзно-кистозной мастопатии.
Основными задачами гинекологов в профилактике и лечении заболеваний МЖ являются [16]: профилактика абортов, особенно повторных абортов;
• своевременное лечение гинекологических заболеваний;
• рациональная контрацепция;
• раннее выявление кистозной мастопатии, лечение патологии МЖ;
• правильное ведение беременности, родов и послеродового периода.
МАСТОПАТИЯ И РИСК РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ
Первоначально ФКБ не рассматривали как патологию, которая имеет отношение к раку МЖ. В дальнейшем, по мере накопления знаний, сформировалось представление о ФКБ как о предраковом состоянии, которое под влиянием определенных обстоятельств трансформируется в рак МЖ. В настоящее время ФКБ рассматривают как один из факторов риска рака МЖ [7, 18]. Предрак МЖ — морфологическое понятие, к нему относят протоковую атипичную гиперплазию эпителия и карциному in situ; дольковую атипичную гиперплазию эпителия и
карциному in situ [25].
В 2006 году в России за 10 лет по сравнению с 1996 годом «грубый» (не стандартизованный по возрасту) и стандартизованный показатель заболеваемости РМЖ на 100 тыс. женского населения выросли соответственно из 30,3% и 16,8%, а «грубый» и стандартизованный показатель смертности — на 16,7 и 3,9% [6]. Такая ситуация отличается от Северной Америки и Западной Европы, где, начиная с 1990-х годов, наблюдается тенденция к снижению смертности от РМЖ. Многие годы в этих странах смертность составляет одну треть от заболеваемости, тогда как в России достигает половины, что объясняется недостаточностью вторичной профилактики, то есть ранней выявляемости РМЖ.
Риск развития рака МЖ на фоне ФКЕ, по мнению многих авторов, зависит от ряда факторов и, в частности, от длительности заболевания. В настоящее время принято считать, что рак МЖ на фоне доброкачественных заболеваний МЖ встречается в 3-5 раз чаще, а при узловой ФКБ с наличием пролиферации эпителия риск рака может повышаться в 30-40 раз. Проведен ряд крупных эпидемиологических когортных проспективных исследований или исследований по методу случай-контроль со средними сроками наблюдения за женщинами от 10 до 20 лет. В качестве контроля для вычисления относительного риска рака МЖ использовались показатели частоты рака МЖ в общей популяции данного региона, среди женщин без ФКБ, с непролиферативной ФКБ. Как наличие ФКБ вообще, так и различные ее формы (аденоз, крупные кисты, радиальные рубцы, внутрипротоковая папиллома, фиброаденома) статистически достоверно повышали риск рака МЖ. ФКБ без пролиферации эпителия повышала риск рака МЖ в 1,27-1,95 раза, ФКБ с гиперплазией безатипии — в 1,53-2,45 раза, ФКБ с атипичной гиперплазией — в 2,03-10,35 раз. При выявлении карциномы in situ риск инвазивного рака МЖ повышается в 8-10 и более раз. Таким образом, риск рака МЖ является минимальным при непролиферативной ФКБ; при пролиферативной ФКБ риск возрастает в 2-4 раза, достигая наиболее высоких цифр при атипичной пролиферации эпителия [7, 13, 29]. В связи с этим, диспансеризация и лечение больных ФКБ с предраковыми изменениями является важным звеном вторичной профилактики рака МЖ.
ФКБ является доброкачественным заболеванием. Однако в ряде случаев данная патология может явиться промежуточной стадией в развитии злокачественного процесса. Учитывая то, что при некоторых формах ФКБ часто встречаются предраковые изменения, при фиброзно кистозной мастопатии лечение и длительное наблюдение за этими пациентками, обеспечивающее профилактику рака МЖ желез, является крайне важным.
ЭТИОПАТОГЕНЕЗ МАСТОПАТИИ
Предполагается, что в основе патологического процесса при ФКБ лежат различного рода гормональные нарушения, проявляющиеся в относительном увеличении уровня эстрогенов, пролактина; нарушении метаболизма эссенциальных жирных кислот, а также другие нарушения [1, 8, 9, 19, 22, 28]. В последние годы изучение роли гормональных факторов в этиопатогенезе заболеваний МЖ приобретает особую актуальность, поскольку признано, что многие формы рака МЖ и ФКБ являются гормонально-зависимыми заболеваниями и развиваются под влиянием множества факторов эндогенного и экзогенного характера.
Главной причиной развития дисгормональных заболеваний МЖ является нарушение соотношения между эстрогенами и прогестероном. Наиболее важную роль в развитии МЖ играет эстрадиол. Его концентрация в соединительной ткани МЖ в 2-20 раз выше, чем в плазме крови. Эстрогены оказывают преимущественно пролиферативное влияние на процессы в МЖ путем прямой стимуляции клеток или опосредованной — через экспрессию полипептидных факторов роста, действующих на эпителий МЖ в качестве ауто- и паракринных стимуляторов пролиферации. Кроме того, стимуляция клеточного роста возможна путем отрицательной обратной связи, согласно которой эстрогены нивелируют эффекты ингибирующих факторов роста [19]. Известно, что эстрадиол стимулирует дифференцировку и развитие эпителия протоков МЖ, усиливает синтез ДНК и митотическую активность эпителия, а в более высоких концентрациях индуцирует формирование ацинуса, стимулирует васкулярицацию, повышает гидратацию соединительной ткани.
Основная роль прогестерона заключается в стимуляции развития альвеол МЖ. Кроме того, прогестерон в пределах эпителия протоков предотвращает пролиферацию и обеспечивает дифференцировку на дольки, тормозит митотическую активность эпителиальных клеток молочных протоков [19]. Под его влиянием в лютеиновую фазу менструального цикла происходит отек и набухание внутридольковой системы, реактивная трансформация эпителия. Именно этим явлением авторы объясняют повышение чувствительности, некоторое нагрубание, увеличение МЖ перед менструацией. Пик митотической активности и продукции ДНК железистой тканью и клетками эпителия в конце лю-геиновой фазы менструального цикла сменяется апоптозом.
Концентрация прогестерона в тканях МЖ в 2-10 раз выше, чем в плазме крови. В ряде случаев вследствие пролиферации эпителия при сохранной секреции в альвеолах развивается обструкция протоков. Со временем это приводит к увеличению альвеол и развитию кистозных полостей. Кроме того, прогестерон ограничивает местное действие эстрогенов на ткань МЖ. Эпителий МЖ содержит фермент 17B-гидроксистероиддегидрогеназу-2, который метаболизирует более активный эстроген эстрадиол в менее активный эстрон. Под влиянием прогестерона повышается активность данного фермента, который инактивирует эстрадиол. Тем самым прогестерон способен снижать экспрессию рецепторов эстрогенов и уменьшить локальный уровень активных эстрогенов в ткани МЖ.
О роли пролактина в патогенезе ФКБ сообщается в многочисленных исследованиях. Известно, что пролактин синтезируется в основном лактотропо-цитами в передней доле гипофиза. Основная функция, которую выполняет пролактин, — это регуляция репродуктивной системы женщины. Доказано, что продукцию и секрецию пролактина стимулируют эстрогены, тиролиберин, гонадолиберин, серотонин, окситоцин, эндогенные опиоиды. Основным ингибитором секреции пролактина через систему 02-рецепторов в мембранах лактотропоцитов является дофамин. Роль пролактина особенно важна при подготовке МЖ к лактации. Именно в этот период в МЖ происходит физиологическая пролиферация и дифференцировка тканей, которая снижается до нормальных показателей после окончания лактации.
По некоторым данным, у большинства пациенток с ФКБ содержание пролактина находится на верхней границе нормы. Другие исследователи указывают на нормальный уровень пролактина у большинства больных ФКБ. Есть данные о наличии у большинства больных ФКБ гиперпролактинемии в сочетании с нарушением функции щитовидной железы [10, 14].
Накоплены многочисленные данные, свидетельствующие о сочетании ФКБ с заболеваниями щитовидной железы [4, 24, 27, 32]. Например, при обследовании в нашем центре 90 женщин с сочетанными гиперплазиями МЖ и гениталий патология щитовидной железы выявлена у 59 (65,5%) [12]. На 8-м Международном противораковом конгрессе было доложено, что у 65% пациенток с диффузной доброкачественной патологией МЖ была выявлена гипофункция щитовидной железы. Эмоциональные стрессы и заболевания нервной системы могут приводить к изменению функционального состояния щитовидной железы. Щитовидная железа существенно влияет на формирование и функционирование репродуктивной системы. На связь репродуктивной и тиреоидной систем указывает изменение активности щитовидной железы в критические периоды женщин: пубертатный период, беременность, актация, климакс. Тиреотрошш-рилизинг-гормон является стимулятором секреции не только тиреотропного гормона (ТТГ), но и пролактина. Стрессовые ситуации, заболевания иммунной системы, инфекции приводят к нарушению биосинтеза ти-реоидных гомонов и, как следствие, к нарушению функции щитовидной железы.
В литературе нет единого мнения в оценке функционального состояния щитовидной железы у больных ФКБ. По мнению одних авторов, гипофункция щитовидной железы повышает риск возникновения ФКБ. Есть данные, что у больных раком МЖ, страдающих гипофункцией щитовидной железы, последняя усугубляется по мере прогрессирования опухолевого процесса. У больных с гипотиреозом часто выявляется ФКБ, особенно ее фиброзная форма. Активация функции щитовидной железы выявлена при пролиферации протокового эпителия. При раке МЖ отмечается снижение функции щитовидной железы, а ТТГ, наоборот, увеличивается.
Таким образом, гормональные нарушения могут предшествовать возникновению ФКБ, и этиопатогенез ФКБ связан с нарушениями не только в репродуктивной системе, но и в центральной нервной системе, печени, надпочечниках, щитовидной железе и других органах [8,9, 23].
КЛИНИКА МАСТОПАТИИ
Масталгия. Основным клиническим проявлением ФКБ являются боли в МЖ, ощущение увеличения их объема, нагрубания (мастодиния). Боли при фиброзной мастопатии молочных желез могут иметь различную интенсивность и характер. У части больных боли могут иррадиировать в подмышечную впадину, плечо, лопатку, шею. Обычно боли в МЖ усиливаются за несколько дней до ожидаемой менструации и прекращаются или уменьшаются после ее окончания. Мастодиния часто сочетается с головными мигренеиодобными болями, отеками, неприятными ощущениями в области живота (ощущение переполнения, метеоризм, запоры), повышенной нервной возбудимостью, раздражительностью, эмоциональной неуравновешенностью, беспокойством, страхом, быстрой утомляемостью, нарушениями сна.
Предменструальный синдром. Наиболее часто ФКБ клинически проявляется также предменструальным синдромом (ПМС), обычно возникающим во вторую (лютеиновую) фазу менструального цикла или за несколько дней до менструации. ПМС также рассматривается как самостоятельный патологический симптомокомплекс, проявляющийся нервно-психическими, вегетативно-сосудистыми и обменно-эндокринными нарушениями. Частота ПМС колеблется в широких пределах и составляет в разные возрастные периоды от 25 до 90% [15].
Этиопатогенез ПМС на сегодняшний день недостаточно изучен, о чем свидетельствует множество теорий, объясняющих механизмы его возникновения. Этиопатогенез ФКБ и ПМС во многом сходен. Наибольшее распространение получила теория психосоматических и вегетативных нарушений. Согласно данной теории, ПМС обусловлен интенсивными нейроэндокринными изменениями в репродуктивной сфере в различные фазы менструального цикла. Эти нарушения, в свою очередь, сопровождаются изменениями функционального состояния вегетативной нервной системы. На электроэнцефалограмме пациенток, страдающих ПМС, отмечены изменения биоэлектрической активности различной интенсивности, причем от степени этих изменений зависят клинические проявления. Важную роль в этиопато-генезе ПМС играют недостаточность витаминов А, В, и Е, дефицит магния, селена, йода, а также реактивная гипогликемия и аллергия.
Всего насчитывается около 150 симптомов ПМС, встречающихся в разных сочетаниях, но наиболее характерными являются следующие: повышенная утомляемость, нагрубание и болезненность МЖ, вздутие живота, тошнота, иногда рвота, нарушение сна и координации, отечность конечностей различной степени выраженности, боли в спине и области таза, увеличение веса, зуд кожи, боли в области сердца, тахикардия. При ПМС также могут отмечаться головная боль, головокружение, запоры, жажда. Нередко пациентки жалуются на изменение вкуса, повышение аппетита, повышение температуры тела, озноб, ухудшение памяти, зрения; может появиться тяга к алкоголю или сладостям. Часто отмечаются раздражительность, плаксивость, депрессия, агрессивность, нерешительность, забывчивость, ипохондрические мысли, мнительность, повышенная требовательность к окружающим, замкнутость, немотивированные страхи, ощущение одиночества, плохое настроение, быстрая смена настроения. Основа диагноза ПМС — циклический характер появления патологических симптомов.
Одним из симптомов ПМС является и мастодиния. Боли в МЖ, как правило, бывают билатеральными, тянущего характера и чаще более выражены в верхненаружных квадрантах и подмышечной области. Масталгия при ПМС носит циклический характер, а при ФКБ может быть и постоянной. Некоторые авторы полагают, что ПМС существенно увеличивает риск развития рака МЖ. По данным французских исследователей, показатель относительного риска возникновения рака МЖ при ПМС может составлять от 2,12 до 5,31 [30, 31].
ЛЕЧЕНИЕ МАСТОПАТИИ
Одной из самых важных составляющих женского здоровья является нормальное функционирование репродуктивной системы. Однако сложная экологическая обстановка, неблагоприятные влияния внешней среды, психические нагрузки, постоянные стрессы, острые инфекционные заболевания, а также неправильное или недостаточное питание зачастую приводят к нарушению функций репродуктивной системы, гормональным изменениям, что проявляется в развитии дисменореи, ФКБ и ПМС; частых сменах настроения, депрессивных состояниях, наступлении раннего климакса. В связи с этим, все острее звучат вопросы повышения качества жизни женщин. И в этом отношении современное лечение является не только залогом сохранения репродуктивного здоровья, но позволяет сохранить физическое и психическое здоровье женщин.
История лечения ФКБ насчитывает более 100 лет, однако единый патогенетический подход к терапии этого заболевания до сих пор отсутствует. Еще не создана единая модель патогененетической терапии, позволяющая дать рекомендации практическому врачу по выбору рациональных медикаментозных комплексов. Остаются совершенно неясными вопросы, касающиеся продолжительности терапии, обеспечивающей нормализацию гормонально-метаболических показателей. Несомненно, лечение больных с доброкачественными заболеваниями МЖ должно быть комплексным, длительным, с учетом гормональных особенностей, сопутствующих экстрагенитальных и гинекологических заболеваний [16,17, 20-22]. Если при обследовании пациентки выявляются узлы или узел в том или ином отделе МЖ, то в этих случаях показано обследование у специалиста (маммолога, хирурга, онколога) с проведением рентгеновской маммографии, пункционной биопсии и других методов обследования для решения вопроса об оперативном лечении. Только диффузные формы ФКБ подлежат консервативному лечению.
Консервативное при кистозной мастопатии лечение имеет своей целью улучшить качество жизни за счет устранения субъективных проявлений болезни и прекращения морфологического прогрессирования процесса. Арсенал средств, предложенных для лечения мастопатии, объединяется в следующие группы:
• диетическое питание и БАД;
• психотропные препараты (седативные, нейролептики);
• нестероидные противовоспалительные средства;
• витамины;
• гомеопатические средства;
• ферментные препараты;
• иммуномодулирующие препараты;
• физиотерапевтические процедуры;
• гормональные препараты.
В течение многих лет препараты йода, сборы трав и комплексы поливитаминов с различной степенью успеха использовались как основные средства для лечения дисгормональной патологии МЖ. Комплексы лекарственных растений обладают мочегонным, седативным, иммуномодулирующим, спазмолитическим, противовоспалительным действием и могут быть рекомендованы пациенткам с ФКБ. В Московском маммологическом диспансере (Клиника женского здоровья) накоплен многолетний положительный опыт лечения ФКБ настойками и отварами специальных сборов лекарственных трав, фито- и гомеопатическими препаратами [3,5]. Однако недостатком фитотерапии является относительная непродолжительность клинического эффекта. В клинической практике в свое время широко и не всегда обосновано использовались йодистые препараты, которые назначались без учета состояния щитовидной железы, поскольку назначение йодотерапии при гиперфункции и другой патологии щитовидной железы может давать ряд побочных эффектов.
Патогенетическим методом терапии ФКБ, учитывая гормональную регуляцию МЖ, следует считать использование гормональных средств. В клинической практике с целью лечения ФКБ наиболее часто используются такие гормональные препараты, как тамоксифен, бромокриптин, даназол, нафарелин, ли-виал; синтетические и натуральные гестагены; производные тестостерона. Правильно подобранная низкодозированная гормональная контрацепция обладает лечебно-профилактическим действием в отношении ФКБ. Следует отметить, что назначение гормональных средств требует тщательного предварительного обследования и правильного подбора препаратов, поскольку при неудачном выборе терапии могут возникать серьезные побочные эффекты, в том числе обострение масталгии, усиление пролиферации тканей МЖ, вплоть до развития узловых образований, возникновения кист [16,22].
Перечисленные сложности обусловливают необходимость поиска новых эффективных лекарственных препаратов с минимальными побочными эффектами, которые могли бы заменить традиционные схемы лечения дисгормональной патологии МЖ.
ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ «МАМОКЛАМ»
Лекарственный препарат «Мамоклам» — таблетки, покрытые оболочкой, 0,1 г, — является новым отечественным негормональным препаратом, разрешенным для медицинского применения в качестве средства для лечения ФКБ (фиброзно-кистозной мастопатии). Мамоклам производят из липидного комплекса бурой морской водоросли ламинарии. Механизмы лечебного действия мамоклама у больных с ФКБ связаны с содержанием в этом средстве йода, полиненасыщенных жирных кислот (ПНЖК) омега-3 типа и хлорофилла. Состав мамоклама на 1 таблетку: йод в органической форме — 100 мкг, ПНЖК омега-3 типа — 40 мг, хлорофилл — 10 мг [2].
Одной из важнейших характеристик мамоклама является наличие в его составе йода, поскольку недостаточность йода в продуктах питания в настоящее время является крайне важной проблемой. Известно, что дефицит йода является одной из причин эндемического зоба, аденом щитовидной железы, гипотиреоза, ожирения, ФКБ и других гормонально-метаболических сдвигов, нервных и психических нарушений, а также фактором, повышающим онкологический риск. Учитывая то, что оптимальное потребление йода взрослым человеком должно составлять 150-200 мкг в сут, мамоклам в рекомендуемой дозе полностью восполняет данный дефицит.
Поступающий с пищей йод накапливается не только щитовидной железой, но и МЖ. В тканях МЖ обнаружены также рецепторы к гормону щитовидной железы трийодтиронину. Йод в тканях МЖ связывается с лииидами, которые регулируют процессы пролиферации клеток МЖ и оказывают антиоксидантное действие. Уменьшение концентрации йода в тканях МЖ имеет большое значение в механизмах развития ФКБ. В клинических исследованиях установлено лечебное действие йода у больных с ФКБ [24,26]. Широко применявшийся ранее в лечении ФКБ йодид калия имеет существенные недостатки: возникновение при длительном приеме явлений йодизма и возможность возникновения индуцированной патологии щитовидной железы, диспептические побочные эффекты и пр. Органически связанный йод в составе мамоклама не имеет этих недостатков.
ПНЖК омега-3 через вмешательство в синтез простагландинов нормализуют баланс половых гормонов, что может объяснять их лечебное действие при ФКБ. ПНЖК омсга-3 обладают также антиканцерогенной и антиметастатической активностью. Хлорофилл — это натуральный антиоксидант, содержащийся в растительной пище, и есть данные, что он тормозит канцерогенез в МЖ, коже и печени.
Хлорофилл обладает антиоксидантным, противовоспалительным, антимутагенным и антиканцерогенным действием, что также имеет отношение к патогенезу ФКБ. Таким образом, мамоклам в результате действия йода, ПНЖК омега-3 и хлорофилла, нормализует баланс тиреоидных и половых гормонов, нормализует процессы пролиферации клеток в ткани МЖ, что оказывает лечебное действие у боль-пых с ФКБ [2].
Биологические эффекты мамоклама также определяют входящие в его состав некоторые макро- и микроэлементы, такие как кальций, магний, цинк, калий, марганец, железо, кобальт, медь, селен. Поскольку известно, что дефицит микроэлементов имеет большое значение в этиопатогенезе различных заболеваний, в том числе и ФКБ, применение данного препарата может иметь большое значение в предупреждении дефицита микроэлементов и связанных с этим заболеваний. Наиболее известным антиканцерогенным микроэлементом, содержащимся в мамокламе, является селен. В многочисленных исследованиях показано, что в регионах с низким содержанием селена в почве, воде и продуктах питания частота рака среди населения значительно выше [2].
Целесообразно проведение, как минимум, двух циклов лечения препаратом «Мамоклам» в год. Дальнейшая тактика лечения будет обусловлена достигнутым эффектом. Вопрос о длительности лечения ФКБ тесно связан с оценкой эффективности проводимой терапии. С клинических позиций целесообразно оценивать эффект лечения по субъективным и объективным критериям. При положительной динамике субъективно пациентки отмечают полное прекращение или уменьшение всех клинических проявлений ФКБ; объективное исследование с помощью инструментальных методов констатирует уменьшение размеров кист, объема увеличенной ткани, а также отека; снижение плотности структуры ткани.
В научно-поликлиническом отделении Научного центра акушерства, гинекологии и перинатологии проведены клинические испытания лекарственного препарата «Мамоклам». Цель исследования: клиническое изучение эффективности лекарственного препарата «Мамоклам» у пациенток с ФКБ.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование были включены 37 женщин позднего репродуктивного возраста. Все пациентки были с сохраненным менструальным циклом. Мамоклам назначался внутрь до еды по 2 таблетки 3 раза в день в течение 3 мес. Обследование пациенток проводилось до и после окончания лечения по следующей схеме: анализ анамнестических данных; осмотр, пальпация МЖ с оценкой клинической симптоматики; рентгенологическое исследование МЖ; эхография МЖ с измерением объема кист. В процессе лечения ежемесячно проводился осмотр и пальпация МЖ с оценкой клинической симптоматики. До конца исследования была прослежена 31 больная. Шесть пациенток были исключены из исследования: 4 — по причине неявки на очередной осмотр врача, 1 — в связи с диспеитическими расстройствами, 1 — в связи с развитием отеков. Все обследования проводили в первой половине менструального цикла. Статистическую обработку результатов проводили стандартными статистическими методами с использованием критериев х2 и точного метода Фишера.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Характеристика больных представлена в табл. 1. Всем пациенткам на основании результатов клинического, эхографического и маммографического обследований был поставлен диагноз: диффузная форма ФКБ; из них у 14 диагностирована ФКБ с преобладанием кистозного компонента, у 11 — с преобладанием фиброзного компонента, у 6 — с преобладанием железистого компонента. Анализ анмнести-ческих данных показал, что у 16 (51,6%) пациенток имелась отягощенная онкологическая наследственность: у ближайших кровных родственников было злокачественные опухоли МЖ или женских половых органов. У подавляющего большинства пациенток имелись указания на инфекционные заболевания в препубертатном и пубертатном периодах. Искусственные аборты в анамнезе отмечены у 27 (87,1%) женщин. У 19 (61,3%) женщин в анамнезе имелись указания на перенесенные ранее гинекологические заболевания, среди которых наиболее часто встречались псевдоэрозии шейки матки — у 11 (35,5%), и хронические воспалительные процессы придатков — у 8 (25,8%). Также наблюдалась высокая частота гиперпластических процессов гениталий у пациенток данной возрастной группы, что отражает известное положение об увеличении с возрастом числа гиперпластических заболеваний женских половых органов. Ведущее место занимала миома матки, которая была у 13 (41,9%) больных (табл. 1).
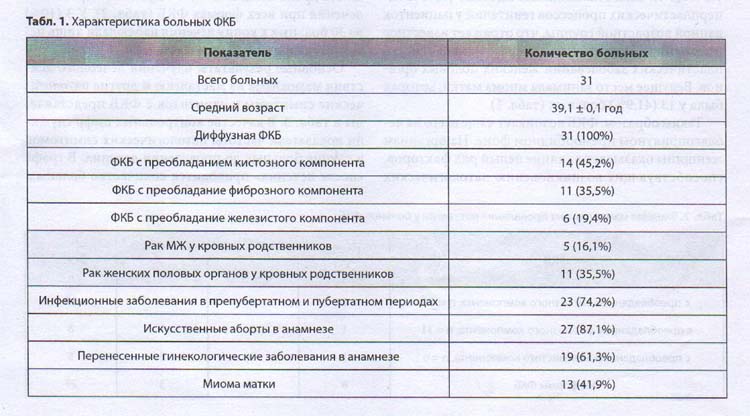
Таким образом, ФКБ возникает чаще всего на неблагоприятном преморбидном фоне. На организм женщины оказывает влияние целый ряд факторов, способствующих возникновению патологических процессов в МЖ: наследственная предрасположенность, перенесенные в детском и пубертатном возрасте инфекционные болезни, искусственные аборты, гинекологические заболевания. Полученные нами анамнестические данные свидетельствуют о неправильности изолированного рассмотрения заболеваний МЖ и о необходимости объединения в единую систему принципов обследования и лечения женщин с болезнями органов репродуктивной системы.
У большинства женщин ранее лечение гиперпластических процессов МЖ не проводилось; 6 (19,4%) женщин получали ранее лечение, состоящее из микродоз йода, витамина А, бромкамфоры, сборов лекарственных трав. Проводимое лечение было несистематическим, не более 3-5 мес, с временным эффектом.
Лечебный эффект лекарственного препарата «Мамоклам» наиболее ярко проявился в отношении масталгии. До лечения на масталгию жаловались 30 (96,8%) из 31 пациентки. У большинства пациенток боли в МЖ наблюдались во второй фазе менструального цикла; из них у 6 (19,4%) боли были постоянные, усиливающиеся перед очередной менструацией; у 10 (32,3%) — отмечалось обострение поверхностной чувствительности в ареолярной зоне за 7-8 дней до предполагаемой менструации. У 27 (90%) из 30 пациенток было отмечено исчезновение симптомов масталгии в течение первых месяцев терапии мамокламом. Лечебный эффект мамоклама проявлялся наиболее выражено через 2 мес лечения при всех формах ФКБ (табл. 2). У 3 (10%) из 30 больных к концу лечения наблюдали лишь незначительное ослабление масталгии.
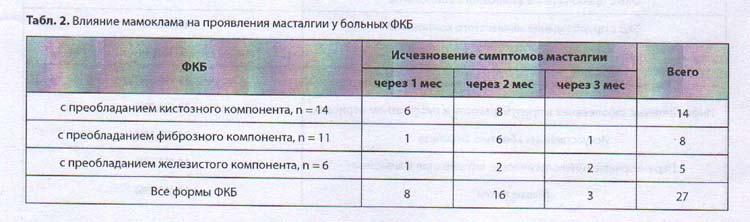
Основные результаты изучения лечебного действия мамоклама на масталгию и другие патологические симптомы у пациенток с ФКБ представлены в табл. 3. В качестве контрольных цифр служили показатели частоты патологических симптомов в группе больных до проведения лечения. В графе «после лечения» приводится количество больных, у которых не наблюдали регрессию патологического симптома.
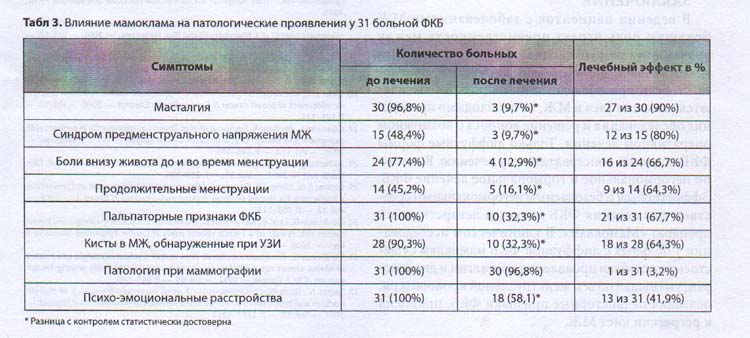
Мамоклам оказывал лечебный эффект на проявления синдрома предменструального напряжения МЖ. До лечения нагрубание и отечность МЖ во второй фазе менструального цикла отмечали 15 (48,4%) из 31 больных. В результате лечения синдром предменструального напряжения МЖ исчезал или ослабевал у 12 (80%) из 15 больных. Мамоклам оказывал лечебный эффект на проявления дисменореи. До лечения боли внизу живота до и во время менструации отмечали 24 (77,4%) больных. У 16 (66,7%) из 24 пациенток проведенное лечение способствовало прекращению и уменьшению болей внизу живота. До лечения у 14 (45,2%) женщин продолжительность менструальных выделений была более 5 дней, достигая 7-8 дней. В результате применения мамоклама у 9 (64,3%) из 14 пациенток уменьшалась продолжительность менструаций, они становились менее обильными, что можно расценивать как положительное влияние мамоклама на клинические проявления менорагии.
Мамоклам оказывал лечебный эффект на паль-паторные признаки ФКБ. До лечения у всех пациенток определялось диффузное уплотнение ткани МЖ в виде напряжения, очагов уплотнений; обычно более выраженное в верхненаружных квадрантах. Часто пальпировались гиперплазированные дольки МЖ различной плотности и эластичности. Большинство пациенток отмечали болезненные ощущения во время пальпации МЖ. После проведенного лечения у 21 (67,7%) из 31 женщин наблюдалось ослабление пальпаторных признаков ФКБ, преимущественно через 3 мес, в виде уменьшения плотности, яжистости и напряжения тканей, а также ослабления болезненности при пальпации. У 10 (32,3%) пациенток динамика пальпаторных признаков ФКБ не наблюдалась.
Лечебный эффект мамоклама проявился в регрессии кист в МЖ. При УЗИ до лечения у всех женщин были выявлены патологические проявления ФКБ, причем у 28 (90,3%) — зарегистрированы кисты. В результате проведенного лечения у 18 (64,3%) из 28 пациенток, по данным повторных УЗИ, наблюдался регресс одной или всех измеренных кист МЖ. При этом у 4 (14,3%) женщин наблюдался полный регресс кист. Кроме того, по сравнению с исходными данными, у 7 из 31 женщин (22,6%) отмечалось снижение эхогенности железистых структур. Вместе с тем, у 10 (35,7%) после проведенного лечения объем кист МЖ не изменился; а у 3 (10,7%) из них наблюдалось незначительное увеличение кист в объеме.
При повторном исследовании после проведенного курса лечения рентгенологическая картина у 30 женщин оставалась стабильной; у 1 (3,2%) пациентки отмечена положительная рентгенологическая динамика, которая заключалась в уменьшении плотности железистого и фиброзного компонентов за счет снижения объема гиперплазированных элементов. Вероятно, при более длительном приеме мамоклама возможен регресс объема гиперпластических структур на маммограммах в большем числе случаев.
До лечения различные психо-эмоциональные расстройства имелись у всех женщин. В результате лечения у 13 (41,9%) пациенток отмечалось положительное влияние мамоклама на психо-эмоциональное состояние, что выражалось в повышении активности, улучшении настроения, исчезновении чувства тревоги, нормализации сна. Все вышеназванные лечебные эффекты мамоклама, за исключением динамики маммографической картины, были статистически достоверными по сравнению с принятыми контрольными показателями (табл. 3).
В целом, мамоклам оказал лечебное действие у 90% пациенток. Ухудшение клинической картины и структуры МЖ по данным маммографии не отмечено пи в одном случае. У всех прослеженных до конца исследования пациенток применение мамоклама не вызывало каких-либо побочных эффектов. Как было сказано выше, у 1 пациентки через 10 дней после приема препарата возникли диспептические расстройства, у 1 — отеки. Следует отметить, что после окончания исследования более 75%жсшцин пожелали продолжить прием мамоклама, что обусловлено не только уменьшением масталгии, предменструального напряжения и нагрубания МЖ, но и значительным улучшением общего состояния.
Результаты проведенного исследования свидетельствуют об эффективности лекарственного препарата «Мамоклам» у пациенток с диффузной ФКБ. Мамоклам оказывал выраженное лечебное действие на все основные субъективные и объективные симптомы ФКБ, нормализовал психоэмоциональное состояние большинства пациенток, давал низкую частоту побочных реакций. Высокая эффективность мамоклама в сочетании с низкой частотой побочных реакций позволяет значительно расширить возможности его применения и считать одним из эффективных средств, полученных из натурального сырья, используемых при лечении ФКБ, что подтверждается полученными нами данными.
ЗАКЛЮЧЕНИЕ
В ведении пациенток с заболеваниями МЖ большую роль играет преемственность между врачами различных специальностей: акушерами-гинекологами, маммологами, хирургами, онкологами. Если при обследовании пациентки выявляются узлы или узел в МЖ, то необходимо проведение обследования и решение вопроса о возможном оперативном лечении. Только диффузные формы ФКБ подлежат консервативному лечению. Возможно негормональное и гормональное лечение ФКБ. Эффективным и безопасным негормональным средством для лечения ФКБ является лекарственный препарат «Мамоклам». В клиническом исследовании у больных с диффузной ФКБ мамоклам существенно ослаблял проявления масталгии и дисменореи, уменьшал объем менструальной кровопотери, ослаблял пальпаторные признаки ФКБ, приводил к регрессии кист МЖ.
ЛИТЕРАТУРА
1. Антипов М. С, Костенко Т. И. Фиброзно-кистозная мастопатия // Журнал прэктич. врача акуш.-гин. — 2003. — № 1. — С. 3-6.
2. Беспалов В. Г. Мастопатия и лекарственный препарат мамоклам. Методическое пособие для врачей. — СПб.: Издательство «Игра света». 2008. — 68 с.
З.Бурдина Л.М. Основные принципы лечения диффузных доброкачественных патологических изменений молочных желез // Маммология. — 1996. — №4.— С 9-14.
4. Горюшина О. Г. Мастопатия / Под ред. В. Ф. Семиглазова. — СПб.: Карэ, 2000. — 109 с.
5. Горячева Л. А., Пинхосевич Е. Г. Фитотерапия при заболеваниях молочных желез.— М, 2006, — 23 с.
6. Злокачественные новообразования в России в 2006 году (заболеваемость и смертность) / Под ред. В. И. Чиссова, В. В. Старинского, Г. В. Петровой. — М.: ФГУ «МНИОИ им. П. А. Герцена Росмедтехнологий», 2008. — 248 с.
7. Зотов А С, Велик Е. О. Мастопагии и рак молочной железы. — М.: МЕДпресс-информ, 2005. —112 с.
8. Ильин А. Б., Бескровный С. В. Молочная железа как орган репродуктивной системы женщины // Акуш. и жен. бол. 2000. — № 2. С. 51-52.
9. Каневцоо В. В. Оптимизация подходов к диагностике и лечению заболеваний молочных желез: Учебно-методическое пособие. — М., 2001.
10. Кира Е. ф., Скрябин О. Н., Цвелев Ю. В. и др. О повышении эффективности диагностики, лечения и профилактики дисфункциональных заболеваний молочных желез // Журнал акуш. и жен. бол. — 2000. — № 1. — С. 95 -99.
11. Коколина В. ф„ Фомина М. А. Заболевания молочных желез у девочек в период созревания репродуктивной системы// Рос. вестник акуш-гин. — 2006. — №4.— С. 17-22.
12. Кулаков В. И., Волобуев А. И., Синицын В. А. и др. Тактика ведения больных с сочетанными доброкачественными гиперплазиями молочных желез и женских половых органов // Маммолог. — 2005. — № 3. С. 4-7.
13. Летягин В. П., Высоцкая И. В., Ким Е. А. Факторы риска развития рака молочной железы // Маммология. — 2006. — № 4. — С. 10-12.
14. Макаренко Н. П. Фиброзно-кистозная болезнь // Рус. мед. журнал. — 2005. — №13 —С. 875-878.
15. Прилепская В. Н., Ме/кееетиново Е. А. Предменструальный синдром // Гинекология. — 2005.—Т. 7, №4.—С. 210 214.
16. Прилепская В. Н.. Швецова О. Б. Доброкачественные заболевания молочных желез: принципы терапии // Маммолог. — 2005. — № 4. — С. 19-25.
17. Радгинский В. Ј., Ордиянц И. М., Зубкин В. И., Иванова Т. Н. Лечение фиброзно-кистозной мастопатии // Фарматека. — 2003. — №11. — С. 46-49.
18. Семиглазов В. Ф., Семиглазов В. В., Клецель А. Е. Неинвазивные и инвазивные опухоли молочной железы. — СПб., 2006. — С. 6-60.
19. Серова О. ф„ Антонова Е. Г. Факторы риска развития фиброзно-кистозной мастопатии в репродуктивном возрасте и современные подходы к ее лечению // Вопр. гииекол. акуш. и перинатол. — 2003. — № 4. — С. 75-79.
20. Сидоренко Л. Н. Мастопатия. — СПб.: Гиппократ, 2007. — 432 с.
21. Тагиева Г. Т. Мастопатия: негормональные методы лечения // Гинекология. — 2004. — Т. 6, № 5. — С. 228-230.
22. Тагиева Т. Т. Фиброзно-кистозная мастопатия//Тамже. 2005. — Т. 7, № 3. — С. 141-144.
23. Хайленко В. А., Легкое А. А., Бурдина Л. М. и др. Дисплазия молочной железы (фиброзно-кистозная болезнь): Методическое пособие для врачей. — М-, 1999.
24. Aceves С, Anguiano В., Delgado G. Is iodine a gatekeeper of the integrity of the mammary gland? // J. Mammary Gland Biol. Neoplasia. — 2005. — Vol. 10. — P. 189-196.
25. Arpino G., laucirico ft., Elledge R.M. Premalignant and in situ breast disease: biology and clinical implications // Ann Intern Med. — 2005. — Vol. 143. — P. 446-457.
26. Conn S.A., van NettenJ.P., van Nelten С Hypothesis: iodine, selenium and the development of breast cancer // Cancer Causes Control. — 2000. —Vol. 11. — P. 121-127.
27. GiustariniE., PincberaA., FierabracciP. etal. Thyroid autoimmunity in patients with malignant and benign breast diseases before surgery // Eur. J, Endocrinol. —
2006. — Vol. 154. — P. 645-649.
28.Miltenburg O.M., Speights V.O. Benign breast disease // Obstet. Gynecol. Clin. North Am. — 2008. Vol. 35. — P. 285 300.
29. OzanneE. M., KlempJ. ft., Euermcm L J. Breast cancer risk assessment and prevention: a framework for shared decision-making consultations // Breast J. — 2006. Vol. 12. —P. 103-113.
30. Plu-Bureau G, LeM. G, Silruk-Ware в., ThalabardJ. С Cyclical mastalgia and breast cancer risk: results of a French cohort study // Cancer Epidemiol. Biomarkers Prev. — 2006— Vol. 15.—P. 1229-1231.
31. Plu-Bureau G., ThalabardJ. C, Sitruk-WareFt. et al. Cyclical mastalgia as a marker of breast cancer susceptibility: results of a case-control study among French women // Br. J. Cancer. — 1992. — Vol. 65. — P. 945-949.
32.Spinos N., Terzis G., Crysanthopoulou A. el at Increased frequency of thyroid nodules and breast fibroadenomas in women with uterine fibroids //Thyroid.
2007. — Vol. 17. — P. 1257-1259.


 English
English